il est constitué d'atome de fer (Fe)

c'est une solution contenant
- l'ion sulfate ![]()
-et l'ion Cu2+.
La couleur bleue de cette solution est caractéristique de la présence d'ion Cu2+
oxydoréduction
première expérience:
| On dispose d'un clou en fer:
il est constitué d'atome de fer (Fe) |
 |
| et d'une solution de sulfate de
cuivre II (CuSO4)
c'est une solution contenant - l'ion sulfate -et l'ion Cu2+. La couleur bleue de cette solution est caractéristique de la présence d'ion Cu2+ |
Plongeons le clou dans la solution et observons:
 |
| D'où vient ce dépôt
rougeâtre sur le clou?
|
Ce n'est pas de la rouille!! |
Ce dépôt est du cuivre métal: Cu, il ne peut donc venir que des ions Cu2+ présents dans la solution de sulfate de cuivre II.
Rappel: l'ion Cu2+ est un atome de cuivre qui a perdu 2 électrons.
Ainsi: L'ion Cu2+ a capté 2 électrons pour "se transformer" en cuivre métal Cu.
Cela s'écrit:  est se nomme une équation électronique (ou
est se nomme une équation électronique (ou
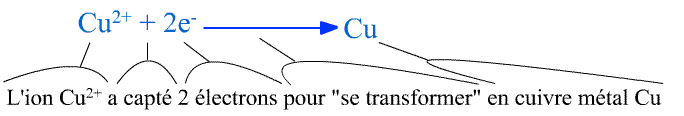
D'où viennent ces deux électrons?
Recommençons l'expérience mais remplaçons le clou de fer par du fer en poudre ou le la laine de fer: cela permet juste d'augmenter la surface de contact entre le fer et la solution de sulfate de cuivre:
|
|
 |
 |
Que se passe-t-il durant cette expérience?
- Il y a bien sur le dépôt de cuivre sur le fer (comme sur le clou) mais le fer étant en poudre, on ne voit pas ce dépôt.
- Par contre, ce qu'on remarquait moins avec le clou, c'est que:
la solution bleue se décolore
Pourquoi?
la couleur bleue est due à la présence d'ions Cu2+, si elle se décolore c'est que ces ions "disparaissent".
En fait, les ions Cu2+ se "transforment" en cuivre métal (atomes Cu) et se dépose sur le fer, nous l'avons déjà vu.
Prélevons un peu de la solution et versons-y quelques goutte de soude :
|
|
 |
 |
| On observe un précipité Jaune-verdâtre caractéristique de la présence d'ions Fe2+ dans la solution |
Ainsi, le fer métal (Fe) s'est "transformé" en ions Fe2+. Il a donc perdu 2 électrons. Voilà d'où viennent les électrons captés les ions ions Cuivre II (Cu2+).
Bilan:
Lorsque l'on plonge du fer (en poudre ou autre...) dans une solution de sulfate de cuivre:
|
|
|
On peut dire qu'il y a eu un transfert d'électrons du fer vers les ions cuivre II |
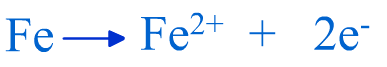 est une réaction d'oxydation: c'est une perte
d'électrons.
est une réaction d'oxydation: c'est une perte
d'électrons.
 est une réaction de réduction: c'est un gain
d'électrons
est une réaction de réduction: c'est un gain
d'électrons
La réaction ![]() n'existe jamais seule: car où iraient les électrons?
n'existe jamais seule: car où iraient les électrons?
De même que la réaction ![]() : car d'où viendraient les électrons?
: car d'où viendraient les électrons?
Ainsi, une réaction d'oxydation s'accompagne toujours d'une réaction de réduction. Elles se "déroulent" en même temps:
Le bilan de ces deux réactions est: une réaction d'oxydo-réduction:
![]()
On y fait pas apparaître les électrons
Les couples Fe/Fe2+ et Cu/Cu2+ forment deux couples oxydoréducteurs
Il se passe quelque chose lorsque l'on plonge du fer dans une solution de sulfate de cuivre:
le fer (métal) est oxydé par l'ion cuivre II
l'ion cuivre II est réduit par le fer (métal)
Et lorsque l'on plonge du cuivre dans une solution de sulfate de fer?
Il ne se passe rien!!!
Le fer réduit les ions cuivre, mais le cuivre ne réduit pas le fer.
On dit que le fer (Fe) est plus réducteur que le cuivre (Cu): il céde plus facilement des électrons.
Deuxième expérience:
| On dispose de cuivre métal:
il est constitué d'atome de cuivre (Cu) |
|
| et d'une solution de nitrate
d'argent (Ag+ +
c'est une solution contenant - l'ion nitrate -et l'ion argent Ag+. |
On introduit le cuivre dans la solution:
|
|
 |
 |
 |
![]() la solution se
colore progressivement en bleu, caractéristique de la présence d'ions Cu2+
dans la solution.
la solution se
colore progressivement en bleu, caractéristique de la présence d'ions Cu2+
dans la solution.
![]() Sur le cuivre, on
observe un dépôt de métal argent
Sur le cuivre, on
observe un dépôt de métal argent
Ainsi:
| Le cuivre a subit une oxydation - Il a été oxydé par les ions Ag+. | |
| Les ions Ag+ ont été réduit en argent métal |
On voit que le cuivre cède 2 électrons: il faut deux ions Ag+ pour "consommer " les deux électrons cédés par le cuivre.
On a ainsi la réaction d'oxydoréduction:
![]()
Et lorsque l'on plonge de l'argent métal dans une solution de sulfate de cuivre?
Il ne se passe rien!!!
Le cuivre réduit les ions Ag+, mais l'argent ne réduit pas le cuivre.
Le cuivre métal est meilleur réducteur que l'argent métal.
Les deux couples oxydoréducteurs en présence sont:
Ag/Ag+ et Cu/Cu2+
On a classé des réducteurs:
Fe est meilleur réducteur que Cu, qui est lui-même meilleur réducteur que Ag.
On peut ainsi classer ces métaux suivant leur pouvoir réducteur:
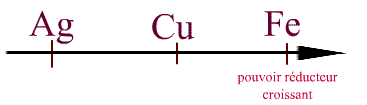
et par là même, les ions suivant suivant leur pouvoir oxydant:
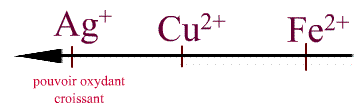
à suivre.....bientôt